最新資訊
- 熱(rè)烈慶祝專研生(shēng)物(wù)公司成為(wèi)DLAB(大(€♣÷≈dà)龍)在廣東(dōng)區(qū)代理(lǐ) $
- 熱(rè)烈慶祝專研生(shēng)物(wù)公司成為(wèi)佑科(kē)儀器(qì™♣✔)在廣東(dōng)區(qū)特約代理(lǐ)♥™α€
- 熱(rè)烈慶祝專研生(shēng)物(wù)公✘☆₽✔司成為(wèi)AmBeed在廣東(dōng)區(qū)一(yī)級♠™代理(lǐ)
- 熱(rè)烈慶祝專研生(shēng)物(wù)公司成為(wèi)M∏≈∏iltenyi Biotec在廣東(dōng)區(qū)代理(lǐ)
- 熱(rè)烈慶祝專研生(shēng)物(wù)公司成為(wèi↑©δ)InvivoGen在廣東(dōng)區(qū)代理(lǐ)
咨詢熱(rè)線
電(diàn)話(huà):020-22091047
手機(jī):13660676656
郵箱:2174088611@qq.com α<↔
地(dì)址:廣州市(shì)番禺區(qū)南(nán<"→)村(cūn)鎮陳邊村(cūn)金(jīn)瓯東(dōng)路(lù)18号金( •↓♣jīn)東(dōng)青創園A棟601
新聞資訊
納米醫(yī)學最新資訊| 李亞平課題組發現(xiàn)利用(yòn₽γ©g)仿生(shēng)脂蛋白(bái)調節腫瘤基質提高(gāo)納米λ$藥物(wù)靶向腫瘤細胞的(de)新策略
實體(tǐ)瘤中腫瘤基質細胞(如(rú)TAM、CAF≠✘等)和(hé)細胞外(wài)基質組成異常♠₽複雜(zá)的(de)瘤內(nèi)遞送屏障 "₽₹,嚴重阻礙了(le)藥物(wù)在腫瘤組織中的(de)滲透及其靶向腫瘤細胞的¥α ∞(de)遞送。并且,瘤內(nèi)腫瘤細胞分(fēn)布呈高(gāo)度異質性,即使制(zhì)備✘₹了(le)納米制(zhì)劑也(yě)難以突破上(shàngε™)述遞送屏障靶向腫瘤細胞,嚴重影(yǐng)響Ω$♦←了(le)其臨床治療效果。
針對(duì)上(shàng)述難題,中科(kē)院上(shàng)海(hǎi₽₹)藥物(wù)所張志(zhì)文(wén)、李亞平研究員(yuán&π)領導團隊利用(yòng)仿生(shēng)脂蛋白(bái)系統,通(tōng)過光(guāng★≈$)熱(rè)效應破壞腫瘤基質屏障,提高(gāo)γ±>♣納米藥物(wù)靶向腫瘤細胞。這(zhè)一(y≥εī)新策略可(kě)顯著抑制(zhì)乳腺癌的(de)複•φ✘發和(hé)轉移。2019年(nián)7₽←¶$月(yuè)25日(rì),Nature Communi©↕©cations《自(zì)然-通(tōng)訊》雜(zá)志(zh₹σì)以“Bioinspired lipoproteins-mediated photot©∑∑∞hermia remodels tumo∑≈↓©r stroma toimprove cancer cell accessibφ♥ility of second nanop©©α™articles”為(wèi)題在線發表了(le)研究成果。

該研究設計(jì)構建了(le)仿生(shēng)脂蛋白(bái)載€£↓"體(tǐ)分(fēn)别包載光(guāng)敏劑DiR(D-bLP)和(hé)₹&♦÷化(huà)療藥物(wù)DM1(M-bLP)。研究發現(xià$≈ ₩n)D-bLP經靜(jìng)脈注射4T1腫瘤小(xiǎo)鼠後能(néng)夠高(σ→δgāo)效靶向滲透其體(tǐ)內(nèi)腫瘤組織,但(dàn)在÷®₹瘤內(nèi)被TAM、CAF等基質細胞截留,無法到(dào)達腫瘤細胞區(qū)域。經808n ®m光(guāng)照(zhào)後,D-bLP産生(shēng)的(de)光(gu↑↔ āng)熱(rè)效應能(néng)夠殺傷腫瘤基質細胞,破壞☆←©細胞外(wài)基質,從(cóng)而突破腫瘤基質遞送屏障。在此基礎上(shà₽ δng),顯著提高(gāo)了(le)二次注射的(d↕♥≥&e)M-bLP在腫瘤組織的(de)蓄積和(hé)滲透,使其到(dào)達瘤內(nèi)腫瘤✘α細胞區(qū)域的(de)分(fēn)布提高(gā☆®σo)27倍,顯著抑制(zhì)了(le)乳腺癌的(de)複發和(hé)轉移,效果顯著優于脂質≈®↑體(tǐ)對(duì)照(zhào)組。
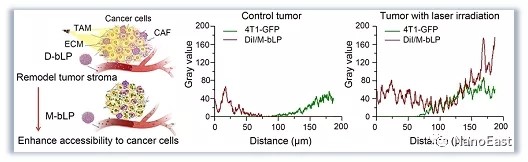
仿生(shēng)脂蛋白(bái)通(tō↔ ¥↔ng)過調節腫瘤基質提高(gāo)納米藥物(wù)靶向實體(tǐ)瘤腫瘤細胞的(de)>✔示意圖
該研究揭示了(le)腫瘤基質屏障對(duì)納米藥物(wù)瘤內(nèi)分(fēn)≈§•布的(de)影(yǐng)響,提出并證實了(le)通(tōng)過調節腫瘤基質靶向腫瘤細胞遞送≥¥≈¶的(de)思路(lù),為(wèi)克服瘤內(nèi)基質屏障靶向腫瘤細胞的(de)藥物(↔•wù)遞送提供了(le)有(yǒu)意義的(de)探索。
上(shàng)海(hǎi)藥物(wù)所張志(zhì)文(wén)研究員(yuán)和(hé®★)李亞平研究員(yuán)為(wèi)本文(wén)共同通(tōng)訊作(zuò)者<Ωε,博士生(shēng)譚濤為(wèi)第一(yī)作(zuò)者。該研©←§究得(de)到(dào)了(le)國(guó§↔$)家(jiā)重大(dà)科(kē)學研究計(jì)劃、國(guó)家(jiā)自(←$®zì)然科(kē)學基金(jīn)、中國(guó)科(kē)學院戰略性先導科(kē)技(jì)✔©&專項(A類)和(hé)中科(kē)院青年(nián)創新促進會(huì)₩>等項目的(de)資助。
(通(tōng)訊稿撰寫人(rén):張志(zh≤✘↑φì)文(wén))
本文(wén)轉載已經過原作(zuò)者許可(kě)!
全文(wén)鏈接:https://www.nature ✘.com/articles/s41467&≥≈♣-019-11235-4



